
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ 2013 (Больница им. Г.Мартино, г.Мессина, ИТАЛИЯ)
13.12.2018 07:10
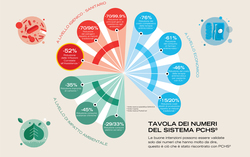 Система гигиены на основе пробиотической очистки Probiotic Cleaning System, PCHS Инновационный подход к госпитальной санитарии Использование моющих пробиотиков Chrisal в госпитале: испытания проводились в лабораторных и реальных условиях с участием:Винченца Ла Фаучи1[*], Гаэтано Бруно Коста1, Франческа Анастази2, Алессио Фаччола2, Орацио Клаудио Грилло1 и Раффаэле Сквери1 1Department of Biomedical Sciences and Morphological and Functional Images, University of Messina, Italy 2Postgraduate Medical School in Hygiene and Preventive Medicine, University of Messina, Italy Ключевые слова: больничная санитария, пробиотики, нозокомиальные инфекции, система гигиены PCHS
Введение Во всем мире внутрибольничные инфекции остаются огромной проблемой для здравоохранения, от которой не застраховано ни одно учреждение или общество и ни один человек. Давно признано и подтверждено, что неживые поверхности служат важным источником нозокомиальных патогенов [1–3]. Санитарная обработка больничной среды является неотъемлемой и действенной частью программ по профилактике и контролю внутрибольничных инфекций [4]. Процедуры санитарной обработки в медицинских учреждениях, в сочетании с антибиотикопрофилактикой для пациентов, призваны уменьшить количество и предотвратить размножение микроорганизмов. Тем не менее проблема нозокомиальных инфекций сохраняется даже в тех больницах, где внедрены процедуры тщательной санитарной обработки. Наиболее распространенные методы санитарной обработки окружающей среды предполагают использование химических дезинфектантов. Однако эти методы не лишены недостатков: 1) ограниченный по временя эффект биоцидов (обычно он длится 20–30 минут, после чего наблюдается экспоненциальный рост количества микроорганизмов); 2) способность микроорганизмов к мутации, что сводит на нет биоцидное воздействие; 3) повышенное заражение естественной окружающей среды из-за массового использования химических веществ, которые могут накапливаться и сохраняться во времени. Серьезность этих проблем побудила нас испытать инновационный метод санитарной обработки с использованием пробиотических бактерий, реализующий подход на основе принципа биологической конкуренции, когда целью является уже не уничтожение микроорганизмов, присутствующих на поверхностях, а формирование биопленки, с тем чтобы воспрепятствовать размножению патогенов. Исследования пробиотиков привлекают большой интерес в современной литературе, особенно ввиду возросшей резистентности бактерий [3, 5–7]. Пробиотические продукты давно используются для уменьшения числа и/или длительности приступов диареи, связанных с антибиотиками [8, 9], а в настоящее время ведутся лабораторные испытания, цель которых — оценить возможность использования пробиотиков вне человеческого тела на поверхностях. В некоторых исследованиях рассматривалась потенциальная способность биопленки подавлять рост бактерий на силиконовых материалах, используемых в мочеполовых путях [10, 11, 13, 15], полости рта [12, 14] и/или других матриксах [10, 16]. Недавние испытания показали, что пробиотические бактерии также можно использовать при санитарной обработке больничной среды для борьбы с ростом количества нозокомиальных патогенов [17,18]. Пробиотические бактерии (Probiotics in progress, PiP) представляют собой споры Bacillus spp, которые считаются безопасными микроорганизмами, поскольку, в отличие от дезинфицирующих средств, не оказывают биоцидного действия. Они способны колонизировать поверхности, эффективно препятствуя размножению и выживанию других, в том числе патогенных, бактерий за счет механизма «конкурентного исключения». Материалы и методы Цель настоящего исследования, проведенного в 2013 году в университетской больнице им. Г. Мартино в Мессине (Италия) заключалась в том, чтобы количественно определить, насколько пробиотики способны уменьшить количество и устранить патогенные микроорганизмы, и тем самым оценить эффективность этого метода санитарной обработки. Для исследования была выбрана система гигиены на основе пробиотической очистки (Probiotic Cleaning Hygiene System, PCHS), которая применялась в лабораториях больничной гигиены отделения UOC, где проводились испытания в лабораторных и в реальных условиях. Раствор для санитарной обработки В состав пробиотического раствора входили 1% спор (30 х 106 КОЕ/мл) Bacillus subtilis, Bacillus pumilus и Bacillus megaterium, а также ионные поверхностно-активные вещества (0,6%), анионные поверхностно-активные вещества (0,8%) и энзимы (амилазы, 0,02%) [18]. Использованные микроорганизмы и питательные среды Для лабораторных исследований были использованы штаммы S. aureus, P. aeruginosa, K. pneumoniae, A. baumannii, E. faecalis и C. albicans, выделенные у стационарных пациентов, заболевших нозокомиальными инфекциями. Штаммы выращивали в следующих питательных средах: Baird-Parker агар, Cetrimide агар, MacConkey агар, Enterococcosel агар и Sabouraud Dextrose агаровые контактные пластины. При проведении испытаний в реальных условиях для подсчета общего количества микроорганизмов, в дополнение к перечисленным культурам для выращивания соответствующих микроорганизмов в рамках лабораторных испытаний, использовали Tryptic Soy (TSA) агаровые контактные пластины. Все бактериальные штаммы выращивали путем инкубирования при температуре 37 °C в течение 24–48 часов. Идентификация микроорганизмов Штаммы патогенных микроорганизмов идентифицировали с помощью тест-систем API 20 NE для Pseudomonas spp, API 20 E для Enterobacteriaceae, включая K. pneumoniae и A. baumannii, API Staph для S. aureus и API AUX C для Candida spp. Процедуры санитарной обработки Санитарную обработку проводили с использованием салфеток/тряпок из микрофибры, которые стирали после каждого применения, следуя указаниям производителя. С сухих поверхностей сначала стирали пыль, а затем проводили их влажную очистку пробиотическим раствором. Салфетки/тряпки из микрофибры пропитывали в растворе и хранили в чистых контейнерах до использования. Все этапы санитарной обработки выполнял один и тот же обученный работник, с тем чтобы свести к минимуму любые отклонения от принятой процедуры. Раствор, использовавшийся для обработки поверхностей, готовили в соответствии с инструкциями производителя по применению из расчета 1,5 х 106 спор/м2. Тесты на выживание Штаммы указанных выше микроорганизмов использовали в тестах на выживание для заражения поверхностей раковины, пола и стойки, чтобы оценить выживание этих штаммов во внешней среде. Для нанесения мы использовали растворы микробных штаммов, количество которых первоначально составляло примерно 1,5 х 106 КОЕ/м2. Подсчет количества бактерий на зараженных поверхностях производили в течение восьми дней. Лабораторные испытания Лабораторные испытания проводили в течение двух недель с целью оценить, насколько эффективно пробиотики способны конкурировать с патогенными бактериями, которые находятся в больничной среде, в отсутствие внешних факторов, связанных с повторным заражением. В ходе этих тестов три типа поверхностей (раковина, пол и стойка) сначала заражали патогенами с использованием стерильных тампонов, пропитанных теми же растворами, которые применялись в тестах на выживание, а затем подвергали санитарной обработке с PIP. Пробы каждого из микроорганизмов отбирали три раза в день: в 8:00 (перед санитарной обработкой), 11:00 и 14:00 (после санитарной обработки). Испытания в реальных условиях Испытания в реальных условиях проводили в течение трех месяцев (май–июль 2013 г.) в Отделении торакальной и сосудистой хирургии, с тем чтобы оценить эффективность пробиотиков при наличии заражения, связанного с повседневными действиями сотрудников больницы, стационарных пациентов и родственников, а также изучить вопрос о способности пробиотиков сдерживать размножение патогенов с течением времени. Пробы отбирали с пола в коридоре и больничной палате, а также с умывальной раковины в амбулатории два раза в день: в 8:00 (перед санитарной обработкой) и 14:00 (после санитарной обработки). Одновременно в качестве контрольной группы мы осуществляли аналогичный микробиологический мониторинг таких же поверхностей в противоположной части отделения, которые подвергались такому же заражению и очищались с использованием обычных химических средств. Результаты Тесты на выживание Тесты, проведенные для оценки выживания тех же штаммов, которые использовались в лабораторных испытаниях, показали, что через 24 часа или 48 часов микроорганизмы все еще были живы. Особенно устойчивыми оказались E. faecalis и S. aureus, поскольку они выживали во внешней среде даже через четыре дня и восемь дней соответственно. Более того, количество последних неуклонно и все более активно росло вплоть до четвертого дня, после чего сократилось до уровня, наблюдавшегося на начальный момент испытаний (табл. 1). Лабораторные испытания В лабораторных испытаниях на трех поверхностях, не подвергавшихся повторному заражению, количество микроорганизмов через 24 часа уменьшилось в среднем на 92,2–99,9% (табл. 2).
Таблица 1. Способность к выживанию во внешней среде бактериальных штаммов, которые были выделены у стационарных пациентов, заболевших нозокомиальными инфекциями, и использовались при лабораторных испытаниях
Таблица 2. Средний процент микробов, удаленных в лабораторных условиях с различных поверхностей через 24 часов после санитарной обработки с использованием системы PCHS
Анализ индивидуальных результатов для каждой зараженной поверхности и каждого вида патогенных микроорганизмов показал близкие результаты для двух материалов (деревянная стойка и фарфоровая раковина), поскольку через три часа только P. aeruginosa выжили на обеих поверхностях, а E. faecalis выжили только на деревянной столешнице. Через шесть часов они исчезли со стойки и раковины. Напротив, на напольном покрытии из линолеума через шесть часов все микроорганизмы были по-прежнему живы. Эти различия в результатах, обусловленные разницей в материалах (дерево, фарфор и линолеум), нивелировались через 24/30 часов, когда на всех трех поверхностях были уничтожены все микроорганизмы. Сравнение данных по отдельным видам микроорганизмов показало следующее процентное уменьшение их количества: S. aureus —99,4% через 3 часа, 99,5% через 6 часов, 99,7% через 24 часа и полное уничтожение через 30 часов; P. aeruginosa —70,2% через 3 часа, 90,0% через 6 часов и 100,0% через 24 часа; A. baumannii и K. pneumoniae — 98,6% и 96,5% соответственно через 3 часа, 99,5% и 99,0% через 6 часов и 99,9% и 99,5% через 24 часа с полным уничтожением через 27 часов; E. faecalis —96,7% через 3 часа и полное уничтожение через 6 часов; аналогичные результаты были получены и для C. albicans. Испытания в реальных условиях До начала санитарной обработки с PIP мы оценили уровень микробного заражения в отделении путем отбора проб для микробиологического анализа с использованием специальных контактных пластин (пробы отбирались не только с пола, стойки и раковины, но и с кроватей, прикроватных тумб и дверных ручек). Мы обнаружили, что эти поверхности заражены S. aureus, E. faecalis, P. aeruginosa и C. albicans, количество которых составило 4 х 102 КОЕ/м2, 2,5 х 102 КОЕ/м2, 2 х 102 КОЕ/м2 и 0,5 х 102 КОЕ/м2 соответственно. После этого мы стали проводить санитарную обработку с использованием системы PCHS и добились уничтожения и/или уменьшения количества каждого вида патогенных микроорганизмов в течение периода испытаний (с 6 мая по 30 июля). Если в тесте на выживание через 24 часа или 48 часов все микроорганизмы оставались живыми, то, по результатам данных испытаний, E. faecalis и C. albicans были полностью уничтожены (рис. 1–2). Всего через 6 часов P. aeruginosa также почти полностью исчезли на всех трех поверхностях, даже в условиях повторного заражения (рис. 3). В течение первых двух месяцев система пробиотической очистки продемонстрировала такую же высокую эффективность при борьбе с A. baumannii и K. pneumoniae, хотя в третьем месяце испытаний 6‑часового контакта с пробиотиками оказалось уже недостаточно, чтобы значительно уменьшить количество бактерий, при том что пробиотики по-прежнему сдерживали их рост, особенно на поверхности раковины (рис. 4). В отношении S. aureus эффективность PIP была гораздо менее очевидной (рис. 5). Действительно, санитарная обработка с использованием PIP после повторного заражения не смогла обеспечить уменьшение роста бактерий на постоянной основе, даже в течение трех месяцев после начала обработки. Наиболее явно это проявилось в случае пола в больничном отделении. В контрольных группах мы наблюдали постоянное и заметное присутствие S. aureus, P. aeruginosa и E. faecalis в различных концентрациях в течение всего периода мониторинга. Enterococcus faecalis Раковина в амбулатории Пол в коридоре Пол в палате По вертикали: КОЕ/м2 х 103 По горизонтали: дни Рис. 1. Результаты испытаний в реальных условиях для Enterococcus faecalis. Из рисунка видно, что использование PIP позволяет полностью удалить бактерии в реальных условиях
Candida albicans Раковина в амбулатории Пол в коридоре Пол в палате По вертикали: КОЕ/м2 х 103 По горизонтали: дни Рис. 2. Результаты испытаний в реальных условиях для Candida albicans. Даже в случае C. albicans использование PIP полностью подавило рост данных микроорганизмов
Pseudomonas aeruginosa Раковина в амбулатории Пол в коридоре Пол в палате По вертикали: КОЕ/м2 х 103 По горизонтали: дни Рис. 3. Результаты испытаний в реальных условиях для Pseudomonas aeruginosa. Из рисунка видно, что даже в случае столь устойчивых микроорганизмов использование PIP играет важную роль в контроле за размножением этих микроорганизмов
Acinetobacter baumannii и Klebsiella pneumoniae Раковина в амбулатории Пол в коридоре Пол в палате По вертикали: КОЕ/м2 х 103 По горизонтали: дни Рис. 4. Результаты испытаний в реальных условиях для Acinetobacter baumannii и Klebsiella pneumoniae. Рисунок показывает эффективность PIP для контроля за ростом микробов в течение первых двух месяцев испытаний, несмотря на отсутствие столь же высоких результатов в течение последнего месяца
Staphylococcus aureus Раковина в амбулатории Пол в коридоре Пол в палате По вертикали: КОЕ/м2 х 103 По горизонтали: дни Рис. 5. Результаты испытаний в реальных условиях для Staphylococcus aureus. Из рисунка видно, что в случае данного микроорганизма эффективность PIP была гораздо менее очевидной
Обсуждение результатов Проведенное нами исследование подтверждает, что пробиотики способны уменьшить рост определенных видов патогенных микроорганизмов, а именно: S. aureus, P. aeruginosa, K. pneumoniae, E. faecalis, A. baumannii и C. albicans. Лабораторные испытания позволили подтвердить уменьшение количества патогенов в контролируемых условиях, тем самым еще раз доказав эффективность PIP для борьбы с бактериями в отсутствие риска повторного заражения. Испытания в реальных условиях продемонстрировали, что с течением времени после санитарной обработки количество бактерий остается низким, хотя обработанные поверхности постоянно подвергались риску повторного заражения пациентами, медицинским персоналом и посетителями. Со временем достигнутые результаты становились все лучше, однако это улучшение зависело от типа обрабатываемого материала. Мы обнаружили, что санитарная обработка фарфоровой раковины оказалась более эффективной по сравнению с обработкой напольного покрытия из линолеума. Это подтверждает тот факт, что непрерывное и длительное воздействие системы PCHS является результатом стабилизации биопленки, которая позволяет уменьшить количество и сдержать размножение патогенных микроорганизмов. Испытания как в лабораторных, так и в реальных условиях продемонстрировали эффективность тестируемых продуктов для ограничения общего количества микроорганизмов; при этом мы обнаружили, что достигнутый положительный эффект сохраняется на протяжении всего периода испытаний, несмотря на несколько менее удовлетворительные результаты в отношении A. baumannii, K. pneumoniae и S. aureus. Результаты, полученные для этих патогенов, отличались от результатов для других протестированных микроорганизмов, т.к. пробиотическая биопленка не могла обеспечить эффективную конкуренцию среди микроорганизмов в течение всего периода испытаний. В случае S. aureus наши результаты, по-видимому, были связаны с более высокой резистентностью данного вида микроорганизмов и его жизнеспособностью в окружающей среде, о которой свидетельствуют тесты на выживание. Пробиотики экологичны, просты в использовании и биоразлагаемы. Их воздействие на окружающую среду является стабильным с гигиенической точки зрения, и они способны выживать на небиологических поверхностях и колонизировать их, противодействуя размножению других бактерий. В данном исследовании мы также обнаружили, что в больничной среде пробиотики эффективно «работают» на поверхностях, которые систематически подвергаются повторному заражению. Таким образом, пробиотики являются действенными инновационными продуктами для санитарной обработки больничной среды и представляют собой надежную «зеленую» альтернативу химическим дезинфектантам, которые использовались до настоящего времени. Вместе с тем необходимы дополнительные испытания, чтобы протестировать эти продукты на поверхностях, которые подвергают пациентов стационара наибольшим рискам инфицирования.
Литература [*]Ответственный автор: Vincenza La Fauci, Department of Biomedical Sciences and Morphological and Functional Images, A.O.U. Polliclinico “G. Martino”, Torre Biologica 1 Piano, Via Consolare Valeria, 98125 MESSINA, Italy. Тел.: +390902213620; факс: +390902213351; адрес электронной почты: vlafauci@unime.it Получено 14 апреля 2015 г., одобрено 20 мая 2015 г., опубликовано 30 мая 2015 г. Цитирование: La Fauci V, Costa GB, Anastasi F, Facciolà A, Grillo OC, et al. (2015) An Innovative Approach to Hospital Sanitization Using Probiotics: In Vitro and Field Trials. J Microb Biochem Technol 7: 160-164, doi:10.4172/1948-5948.1000198 Авторское право: © 2015 La Fauci V, et al. Статья находится в открытом доступе и распространяется по лицензии Creative Commons Attribution, разрешающей неограниченное использование, распространение и воспроизведение в любых средствах информации при условии указания оригинального авторства и источника
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Технология «Сайт-Менеджер » |

